وزارت بهداشت، درمان و آموزش پزشکی به منظور بهرهبرداری بهتر و سازماندهی امکانات و تجهیزات پزشکی و تأمین و تعمیم بهداشت، درمان، بهزیستی، آموزش و پژوهش در سال 1364 تشکیل شد. ذیل این وزارتخانه، نه(9) معاونت قرار دارد؛ یکی از این معاونتها، معاونت غذا و دارو میباشد. در سال 1358 بخشهای مرتبط با تجهیزات پزشکی و امور آزمایشگاهی به این معاونت اضافه شدند و معاونت دارویی، غذایی و آزمایشگاهی نامیده شد و در نهایت سازمان غذا و دارو در سال 1389 با تصویب شورای عالی اداری به منظور هدایت و نظارت بر امور غذایی و دارویی تشکیل شد. این سازمان از معاونت نظارت و ارزیابی، معاونت فنی و معاونت توسعه مدیریت و منابع تشکیل شده است که مسئولیت صدور مجوزها بر عهده دو معاونت نظارت و ارزیابی و معاونت فنی میباشد. معاونت نظارت و ارزیابی شامل چهار (4) اداره کل امور دارو و مواد تحت کنترل، امور فرآوردههای آرایشی و بهداشتی، امور فرآوردههای طبیعی، سنتی و مکمل و امور فرآوردههای غذایی و آشامیدنی میباشد و معاونت فنی نیز شامل اداره کل امور تجهیزات و ملزومات پزشکی، اداره کل آزمایشگاههای مرجع کنترل غذا، دارو و تجهیزات پزشکی و دفتر نظارت و پایش مصرف فرآوردههای سلامت میباشد.
بخشی از وظایف این سازمان را در ادامه این مقاله میتوانید ملاحظه کنید:
- تدوین، ارائه و ابلاغ سیاستها، برنامهها و خط مشیهاي مواد و فرآوردههای تحت نظارت سازمان؛
- سیاستگذاری، برنامهریزی و اجرای پژوهشهای مرتبط با نظارت، آزمایش، کنترل کیفی، ایمنی، سلامت و ارتقای کیفیت مواد و فرآوردههای تحت نظارت سازمان؛
- تعیین، تدوین و اعلام استانداردها، ضوابط، ویژگیها و مقررات مربوط به واردات، صادرات، تهیه، تولید، کنترل، آزمایش، نگهداری، انبارش، حمل و نقل، توزیع، عرضه، مصرف و انهدام مواد و محصولات و فرآوردههای تحت نظارت سازمان؛
- تعیین، تدوین و اعلام ضوابط و ویژگیهای مربوط به نظارت و کنترل بر برنامهها و خدمات واحدهای مربوطه؛
- صدور، تمدید و لغو موقت و دائم پروانه مؤسسات تولیدی، وارداتی، صادراتی، نگهداری، انبارش، حمل و نقل، عرضه و توزیع مواد و فرآوردههای تحت نظارت سازمان؛
- صدور پروانهها و مجوزهای بهداشتی ساخت، صادرات، ورود، مصرف و انهدام مواد و فرآوردههای تحت نظارت سازمان؛
لازم به ذکر است گستره فعالیت این سازمان در راستای اهداف فوق، شامل مواد و فرآوردههای دارویی، غذایی، طبیعی، آشامیدنی، آرایشی و بهداشتی، بیولوژیک، مکملها، فرآوردههای مرتبط حاصل از فنآوريهاي نوین، مواد و داروهای تحت کنترل، شیرخشک، اقلام، تجهیزات و ملزومات پزشکی و دندانپزشکی مصرفی و غیرمصرفی، اقلام بستهبندی، لوازم و اسباببازی کودک میباشد.
سازمان غذا و دارو اقدام به صدور مجوزهای لازم برای فعالیت شرکتها و واحدهای تولیدی میکند؛ مجوزهایی که این سازمان در دو حوزهی دارو و آرایشی بهداشتی صادر میکند، به شرح ذیل میباشد.
- حوزه دارو:
- صدور مجوز فعالیت شرکت دارویی: مناسب شرکتهای متقاضی ثبت دارو بصورت تولید داخلی، قراردادی و تحت لیسانس و واردات؛
- صدور موافقت اصولی احداث کارخانه داروسازی: مناسب شرکتهای متقاضی تولید دارو؛
- صدور و تمدید پروانه مسئولین فنی شرکتهای تولید کننده، وارد کننده، فرآورده های بیولوژیک، مواد اولیه دارویی، ملزومات دارویی و داروهای تحت کنترل: مناسب شرکتهای متقاضی تولید دارو، واردات دارو، فرآورده های بیولوژیک، مواد اولیه، ملزومات دارویی و داروهای تحت کنترل؛
- صدور پروانه تأسیس کارخانه داروسازی برای داروهای شیمیایی و واحدهای بستهبندی بالکهای دارویی: مناسب شرکتهای داروسازی دارای موافقت اصولی احداث کارخانه؛
- مجوز تولید قراردادی (داخلی): مناسب شرکتهای تولید کننده دارو؛
- ثبت درخواست تولید تحت لیسانس: مناسب شرکتهای واردکننده و تولیدکننده دارو؛
- ثبت درخواست تولید قراردادی برون مرزی: مناسب شرکتهای دارای مجوز فعالیت شرکت دارویی، موافقت اصولی احداث، پروانه تاسیس؛
- صدور پروانه ثبت تولید داخل: مناسب شرکتهای دارویی؛
- تمدید و اصلاح پروانه ساخت دارو: مناسب شرکتهای دارویی؛
- صدور پروانه ثبت (داروهای وارداتی): مناسب شرکتهای دارویی؛
- کمیته نامگذاری داروها: مناسب شرکتهای تولیدکننده دارو؛
وظیفه بررسی درخواستها و صدور پروانهها و مجوزهای مذکور به عهده اداره ثبت و صدور پروانه اداره کل نظارت و ارزیابی دارو و مواد مخدر میباشد. فرایند کلی اخذ مجوز و پروانههای دارویی مطابق شرح ذیل است:
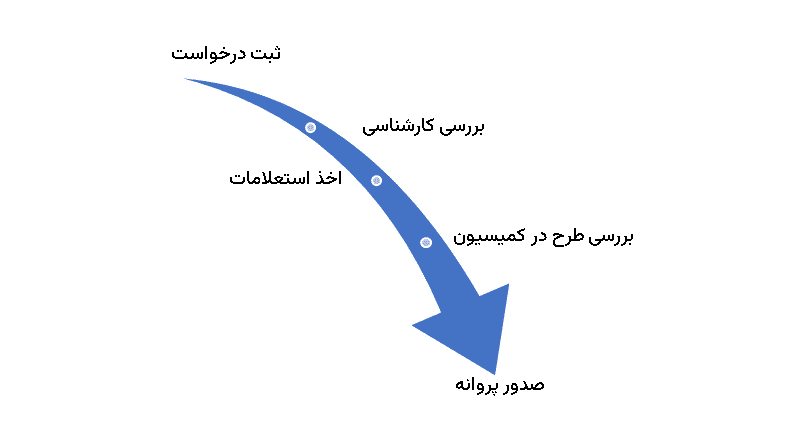
- حوزه غذا، آرایشی و بهداشتی:
- صدور، اصلاح و تمدید پروانههاي بهداشتی برای شرکتهای نگهداري، پخش و توزیع فرآوردههاي غذایی، آرایشی و بهداشتی؛
- صدور، اصلاح و تمدید پروانه بهداشتی ساخت فرآوردههای آرایشی و بهداشتی؛
- صدور و تمدید پروانه مسئولین فنی شرکتهای واردکننده مواد اولیه؛
فرایند دریافت گواهی بهداشت محصولات آرایشی و بهداشتی:
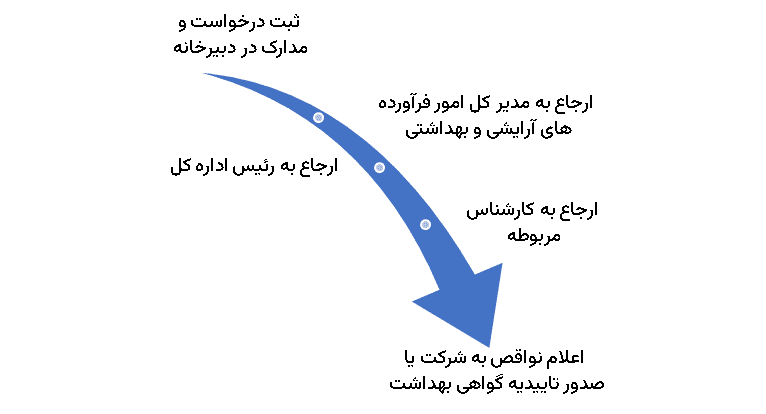
- حوزه تجهیزات پزشکی:
- صدور کد ثبت برای تجهیزات پزشکی تولید داخل و وارداتی
مراحل اخذ کد ثبت تجهیزات پزشکی توسط اداره کل تجهیزات پزشکی به شرح ذیل میباشد:
- ارائه درخواست الکترونیکی ثبت تجهیزات پزشکی ، تعیین کلاس خطر، تکمیل مدارک و ارائه مستندات؛
- بررسی اولیه تطابق با الزامات فنی مورد تأیید کمیته فنی؛
- بررسی ایمنی و عملکرد؛
- بررسی مستندات؛
- بررسی در کمیته تخصصی؛
- بررسی شرایط تولید و بازدید میدانی؛
- ارزیابی فناوری سلامت (HTA)،
- بررسی آزمایشگاهی نمونه؛
- ارزیابی بالینی؛
- اثبات خلاف ادعای سازنده؛ چنانچه سازنده قانونی (وارداتی) و یا نماینده آن در ابتدا ادعای تطابق با الزامات اساسی اصول ایمنی و عملکرد و الزامات فنی را داشتهاست، چنانچه نتایج راستی آزمایی ارزیابی بالینی یا آزمایشگاهی نمونههای وارداتی در داخل کشور، با ارزیابیهای پس از ورود به بازار مردود باشد یا اشکالات اساسی مشاهده شده باشد، فرصت اصلاح نمونه و درخواست ثبت مجدد تجهیزات پزشکی وارداتی امکانپذیر نمیباشد
فرآیند کد ثبت برای تجهیزات پزشکی تولید داخل و وارداتی:
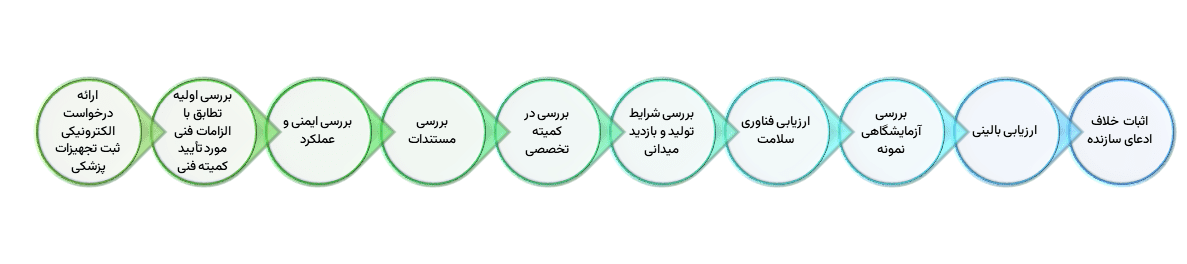
شرکت توسعه نوآوری و فناوری تدبیرسینا با کمک کارشناسان و مشاوران با تجربه در این مسیر در کنار شماست تا فرایند دریافت مجوز را کوتاهتر و آسانتر طی کنید.
برای کسب اطلاعات بیشتر و دریافت مشاوره میتوانید از طریق شماره تماسهای موجود در سایت با کارشناسان ما در ارتباط باشید.


